ADHS
ADHS und Blutwerte: Welche Mikronährstoffe wirklich fehlen
11. April 2026 · Von Dr. B.J. Huber · 25 Min. Lesezeit
Dein Gehirn braucht Rohstoffe. Und bei ADHS fehlen oft genau die richtigen.
ADHS wird in der Regel als Neurotransmitter-Problem beschrieben: zu wenig Dopamin, zu wenig Noradrenalin, gestörte Signalübertragung im präfrontalen Kortex. Das stimmt. Aber es ist nur die halbe Geschichte.
Damit dein Gehirn Dopamin, Serotonin und Noradrenalin überhaupt herstellen kann, braucht es Rohstoffe: Eisen, Zink, Magnesium, B-Vitamine, Omega-3-Fettsäuren, Vitamin D und bestimmte Aminosäuren wie Tyrosin und Tryptophan. Und damit diese Neurotransmitter stabil arbeiten, braucht es ein Nervensystem, das nicht permanent unter oxidativem Stress steht, und einen Darm, der Nährstoffe aufnimmt, statt Entzündungssignale ins Gehirn zu schicken. Diese biologischen Stellschrauben sind Teil der grösseren Longevity-Grundlagen, die auf Zellalterung auf messbarer Ebene wirken.
Die Forschung der letzten Jahre zeigt ein konsistentes Muster: Menschen mit ADHS haben in mehreren dieser Bereiche messbare Abweichungen. Nicht alle, nicht immer die gleichen, aber statistisch signifikant häufiger als die Allgemeinbevölkerung. Das ist kein Zufall, sondern hat biologische Gründe. Besonders relevant ist dabei Magnesium: Magnesium L-Threonat als spezifische Form zeigt bei ADHS besondere Wirksamkeit, weil es die Blut-Hirn-Schranke überwindet.
Dieser Artikel gibt dir eine Übersicht: Welche Blutwerte und Darmparameter bei ADHS oft nicht im optimalen Bereich liegen, warum das so ist, und was du konkret testen lassen kannst.
- Medikamente erhöhen Dopamin, aber ohne Magnesium, Eisen, Zink und B-Vitamine kann das Gehirn es gar nicht erst herstellen.
- Dein Standard-Blutbild versteckt intrazelluläre Mängel — ein normaler Serum-Magnesiumwert schliesst einen Mangel in deinen Zellen nicht aus.
- Bei ADHS ist ein gestörtes Darmmikrobiom häufig, das Entzündungssignale ins Gehirn sendet und damit ADHS-Symptome verstärkt.
Magnesium: Der NMDA-Blocker, der fast immer fehlt
Magnesium ist der Mikronährstoff, der bei ADHS mit Abstand am besten untersucht ist. Eine Metaanalyse von Effatpanah et al. (2019), die sieben kontrollierte Studien auswertete, fand signifikant niedrigere Serum-Magnesiumspiegel bei Menschen mit ADHS im Vergleich zu gesunden Kontrollen (Differenz: -0,105 mmol/L, p < 0,013). Eine weitere Metaanalyse von Huang et al. (2019) bestätigte diesen Befund sowohl für Serum- als auch für Haar-Magnesiumwerte.
Die Zahlen sind noch drastischer, wenn man intrazelluläre Messungen betrachtet: Kozielec und Starobrat-Hermelin (1997) fanden bei 95 Prozent der untersuchten ADHS-Kinder einen Magnesiummangel, am häufigsten in den Haaren (77,6 Prozent), gefolgt von Erythrozyten (58,6 Prozent) und Serum (33,6 Prozent). Das zeigt ein wichtiges Prinzip: Der Serumwert ist bei Magnesium ein schlechter Indikator für den tatsächlichen Versorgungsstatus.
Warum fehlt Magnesium bei ADHS?
Drei Mechanismen greifen ineinander. Erstens: Stress verbraucht Magnesium. Bei ADHS ist das autonome Nervensystem dauerhaft in Richtung Sympathikus verschoben, was den Magnesiumverbrauch erhöht. Pickering et al. (2020) zeigten, dass diese Beziehung bidirektional ist: Stress senkt Magnesium, und Magnesiummangel verstärkt die Stressreaktion. Zweitens: Stimulanzien wie Methylphenidat verändern das Calcium-Magnesium-Verhältnis und können die renale Magnesiumausscheidung erhöhen (Schmidt et al., 1994). Drittens: ADHS-bedingte Ernährungsgewohnheiten (impulsives Essen, verarbeitete Lebensmittel, reduzierter Appetit unter Medikation) führen häufig zu einer unzureichenden Zufuhr.
Was Magnesium im ADHS-Gehirn macht: Es ist der natürliche Blocker des NMDA-Rezeptors und schützt vor Glutamat-Exzitotoxizität, also der Überstimulation von Nervenzellen, die bei ADHS ein zentrales Problem darstellt (Sartori et al., 2012).
Empfohlene Tests: Serum-Magnesium (Mindeststandard), besser: Vollblut-Magnesium oder intrazelluläre Mineralstoffanalyse, da der Serumwert einen intrazellulären Mangel nicht ausschliesst.
Eisen und Ferritin: Der Dopamin-Cofaktor
Eisen ist ein essenzieller Cofaktor der Tyrosinhydroxylase, des Schlüsselenzyms der Dopaminsynthese. Ohne ausreichend Eisen kann das Gehirn nicht genug Dopamin produzieren, und genau das ist das Kernproblem bei ADHS.
Eine Metaanalyse von Cortese et al. (2012) und eine systematische Übersichtsarbeit von Wang et al. (2017), veröffentlicht in Scientific Reports, fanden übereinstimmend: Serum-Ferritin-Werte sind bei Kindern mit ADHS statistisch signifikant niedriger als bei gesunden Kontrollen, mit einer moderaten Effektgrösse. Interessanterweise war der Serum-Eisenwert selbst nicht signifikant unterschiedlich, was darauf hindeutet, dass die Eisenspeicher (Ferritin) das relevantere Mass sind.
Warum ist Ferritin bei ADHS niedrig?
Die Forschung deutet auf mehrere Ursachen hin. Erstens spielt die genetische Variation im Eisenstoffwechsel eine Rolle: Polymorphismen in Genen, die den Eisentransport regulieren, könnten das Risiko erhöhen. Zweitens ist die Aufnahme oft eingeschränkt: Stimulanzien unterdrücken den Appetit, was über Monate zu einer reduzierten Eisenzufuhr führen kann. Drittens verbrauchen chronische unterschwellige Entzündungsprozesse, die bei ADHS häufiger vorkommen, Eisen.
Ein wichtiger Punkt: Ferritinwerte, die im Referenzbereich liegen (z. B. 30 ng/mL), können funktionell trotzdem zu niedrig sein. Einige ADHS-Forscher halten Ferritinwerte unter 45 ng/mL bereits für suboptimal für die Dopaminsynthese.
Empfohlene Tests: Ferritin (nicht nur Hämoglobin), Transferrinsättigung, CRP (um entzündungsbedingt falsch-hohe Ferritinwerte auszuschliessen).
Zink: Mehr als ein Spurenelement
Zink spielt eine zentrale Rolle bei der synaptischen Signalübertragung und ist ein Cofaktor für über 300 Enzyme, darunter solche, die an der Neurotransmittersynthese beteiligt sind. Es moduliert Dopamin- und Melatoninrezeptoren und beeinflusst die GABA-Signalgebung.
Eine Metaanalyse von Ghoreishy et al. (2021), veröffentlicht in Scientific Reports mit 22 Studien (1.280 ADHS-Probanden, 1.200 Kontrollen), fand niedrigere Zinkblutspiegel bei ADHS-Betroffenen, obwohl die Ergebnisse statistisch heterogen waren. Auch Skalny et al. (2020) bestätigten in ihrer Analyse signifikant niedrigere Zink- und erhöhte Kupfer/Zink-Verhältnisse bei ADHS.
Warum ist Zink bei ADHS niedrig?
Zink wird bei Stress verstärkt ausgeschieden. Das ADHS-typische chronische Stressniveau erhöht den Zinkbedarf. Gleichzeitig konkurriert Kupfer mit Zink um die Aufnahme im Darm. Wenn Kupfer erhöht ist (was bei ADHS häufiger vorkommt), wird die Zinkaufnahme zusätzlich beeinträchtigt. Auch hier spielen Ernährungsgewohnheiten und Appetitreduktion durch Medikamente eine Rolle.
Empfohlene Tests: Serum-Zink, Kupfer, Kupfer/Zink-Ratio.
Kupfer: Wenn ein Spurenelement zu hoch ist
Während die meisten Mikronährstoffe bei ADHS zu niedrig sind, ist Kupfer oft erhöht. Das ist kein Widerspruch, sondern Teil desselben Ungleichgewichts.
Kupfer ist Cofaktor der Dopamin-Beta-Hydroxylase, des Enzyms, das Dopamin in Noradrenalin umwandelt. Zu viel Kupfer bedeutet: zu viel Noradrenalin. Noradrenalin-Überschuss erzeugt Hyperaktivität, Impulsivität, Reizbarkeit und Aggressivität, also klassische ADHS-Symptome.
Skalny et al. (2020) fanden bei Jungen mit ADHS signifikant erhöhte Kupfer/Zink-Verhältnisse, wobei die Kupferwerte 12 Prozent über den Kontrollwerten lagen, primär getrieben durch einen 7-Prozent-Abfall im Serum-Zink. Arnold et al. (2005) zeigten zudem, dass Kinder mit erhöhtem Kupfer schlechter auf Stimulanzien ansprechen. Der Grund: Stimulanzien erhöhen Dopamin, das durch überschüssiges Kupfer sofort in Noradrenalin umgewandelt wird, was die Symptomatik verschärft statt sie zu lindern.
Warum ist Kupfer bei ADHS erhöht?
Die Ursachen sind multifaktoriell. Kupfer-Zink-Antagonismus: Wenn Zink fehlt, steigt Kupfer relativ an. Östrogen erhöht die Kupferspiegel, was erklären könnte, warum manche Frauen mit ADHS zyklusabhängige Symptomverschlechterungen erleben. Stress und Entzündungen erhöhen Ceruloplasmin, das wichtigste Kupfer-Transportprotein.
Empfohlene Tests: Serum-Kupfer, Ceruloplasmin, Kupfer/Zink-Ratio.
Vitamin D: Neuroprotektiv und fast immer zu niedrig
Vitamin D ist streng genommen kein Vitamin, sondern ein Neurohormon. Es reguliert über 1.000 Gene, darunter solche, die an der Neuroprotektion, der Immunregulation und der Neurotransmittersynthese beteiligt sind.
Eine Metaanalyse von Khoshbakht et al. (2018) mit Daten von über 10.000 Kindern und Jugendlichen fand, dass Kinder mit ADHS signifikant niedrigere 25(OH)D-Spiegel haben als gesunde Kontrollen (gewichtete Mitteldifferenz: -6,75 ng/mL). Alle acht eingeschlossenen Studien zeigten diesen Effekt. Eine weitere Analyse von fünf Fall-Kontroll-Studien ergab: niedrige Vitamin-D-Spiegel sind mit einem 2,57-fach erhöhten ADHS-Risiko assoziiert. Besonders bemerkenswert: Niedrige perinatale Vitamin-D-Konzentrationen waren mit einem 40 Prozent höheren ADHS-Risiko im späteren Leben verbunden.
Warum ist Vitamin D bei ADHS niedrig?
Menschen mit ADHS verbringen oft mehr Zeit in Innenräumen (Bildschirmzeit, Schwierigkeiten bei der Alltagsorganisation). Dazu kommen Ernährungsdefizite und in nördlichen Breitengraden generell unzureichende Sonneneinstrahlung. Es gibt auch Hinweise auf genetische Varianten im Vitamin-D-Stoffwechsel, die bei ADHS häufiger auftreten.
Empfohlene Tests: 25(OH)D (25-Hydroxyvitamin D). Optimalwerte liegen bei 40 bis 60 ng/mL, nicht nur über dem Referenzbereich von 30 ng/mL.
Omega-3-Fettsäuren: Baustoff der Zellmembranen
Omega-3-Fettsäuren, insbesondere EPA und DHA, sind essenziell für die Struktur und Funktion neuronaler Zellmembranen. DHA macht etwa 20 Prozent der Fettsäuren im Gehirn aus und ist entscheidend für die Fluidität synaptischer Membranen, die wiederum die Rezeptorfunktion beeinflusst.
Eine Metaanalyse von Chang et al. (2018), veröffentlicht in Neuropsychopharmacology, fasste die Ergebnisse zusammen: Kinder und Jugendliche mit ADHS haben signifikant niedrigere Blutspiegel von EPA und DHA als Kontrollen, mit einer moderaten Effektgrösse von einem Drittel bis einer halben Standardabweichung. Besonders auffällig war das Omega-6/Omega-3-Verhältnis: LaChance et al. (2016) fanden in ihrer Metaanalyse, dass ADHS-Betroffene ein signifikant erhöhtes Omega-6/Omega-3-Verhältnis und ein erhöhtes AA/EPA-Verhältnis aufweisen.
Warum sind Omega-3-Werte bei ADHS niedrig?
Die westliche Ernährungsform enthält typischerweise ein Omega-6/Omega-3-Verhältnis von 15:1 bis 20:1, statt des evolutionär angepassten 1:1 bis 4:1. Bei ADHS kommt hinzu: impulsives Essverhalten bevorzugt oft verarbeitete, omega-6-reiche Lebensmittel. Es gibt auch Hinweise auf Polymorphismen in den Desaturase-Genen (FADS1, FADS2), die die Umwandlung von ALA zu EPA und DHA beeinträchtigen können und bei ADHS häufiger vorkommen.
Ein wichtiger Hinweis zur Supplementierung: Bei ADHS wird häufig ein höherer EPA-Anteil im Verhältnis zu DHA empfohlen (z. B. 2:1 oder höher), da EPA stärker anti-neuroinflammatorisch wirkt. Die Supplementierungsstudien, die bei ADHS positive Effekte zeigten, verwendeten typischerweise EPA-dominante Präparate mit einer Behandlungsdauer von mindestens vier Monaten.
Empfohlene Tests: Omega-3-Index (Zielwert: 8 bis 11 Prozent), AA/EPA-Ratio.
B-Vitamine und Homocystein: Der Methylierungskreislauf
B-Vitamine, insbesondere B6 (Pyridoxin), B9 (Folat) und B12 (Cobalamin), sind Schlüsselfaktoren im Methylierungszyklus, der direkt die Synthese von Dopamin, Serotonin und Noradrenalin steuert.
Eine Studie von Altun et al. (2018), veröffentlicht in der Zeitschrift für Kinder- und Jugendpsychiatrie, fand bei Kindern mit ADHS signifikant niedrigere Serumspiegel von B6, B12 und Folat als bei Kontrollen. Yektaş et al. (2019) verglichen in einer kontrollierten Studie die Serumspiegel von 48 ADHS-Kindern mit gesunden Kontrollen und fanden signifikant niedrigere B12-Werte und erhöhtes Homocystein in der ADHS-Gruppe. B12-Spiegel korrelierten negativ mit Hyperaktivitäts- und Impulsivitätssymptomen. Homocystein ist ein Marker für die Effizienz des Methylierungszyklus: Wenn es erhöht ist, funktioniert die Methylierung nicht optimal.
Warum sind B-Vitamine bei ADHS oft suboptimal?
Hier kommt die Genetik ins Spiel. Polymorphismen im MTHFR-Gen (Methylentetrahydrofolatreduktase) reduzieren die Fähigkeit, Folat in seine aktive Form Methylfolat umzuwandeln. Methylfolat ist das Schlüsselmolekül, das Homocystein zu Methionin recycelt und damit den gesamten Methylierungszyklus antreibt. Studien zeigen, dass bestimmte MTHFR-Varianten (C677T und A1298C) bei ADHS überrepräsentiert sein könnten. Dazu kommen die üblichen Verdächtigen: Appetitverlust durch Stimulanzien, einseitige Ernährung, und ein stressbedingt erhöhter Verbrauch.
Empfohlene Tests: Homocystein, Vitamin B12 (Holotranscobalamin ist sensitiver als Gesamt-B12), Folat (Erythrozytenfolat ist aussagekräftiger als Serumfolat), Vitamin B6.
Aminosäuren: Die direkten Bausteine deiner Neurotransmitter
Aminosäuren sind die unmittelbaren Vorstufen von Dopamin, Serotonin und Noradrenalin. Ohne sie kann das Gehirn diese Botenstoffe schlicht nicht produzieren, egal wie gut die Mikronährstoffversorgung ist. Die Forschung zeigt, dass bei ADHS mehrere Aminosäure-Pfade messbar verändert sind.
Tyrosin und Phenylalanin: Die Dopamin-Kette
Phenylalanin wird zu Tyrosin umgewandelt, und Tyrosin ist die direkte Vorstufe von L-DOPA, aus dem Dopamin entsteht. Das ist die Kern-Kaskade bei ADHS.
Bornstein et al. (1990) fanden in einer der frühesten Studien zum Thema signifikant niedrigere Plasma-Spiegel von Tyrosin, Phenylalanin, Tryptophan, Histidin und Isoleucin bei 28 ADD-Patienten gegenüber 20 Kontrollen. Die Autoren interpretierten das als Hinweis auf einen generellen Defekt im Aminosäuretransport oder in der Absorption.
Neuere Forschung (Bergwerff et al., 2016, 83 ADHS-Kinder vs. 72 Kontrollen) fand allerdings keine signifikanten Unterschiede bei den aromatischen Aminosäuren im Blut. Das klingt widersprüchlich, ergibt aber aus biochemischer Sicht Sinn: Das Problem liegt wahrscheinlich weniger im Plasmaspiegel als im Transport über die Blut-Hirn-Schranke. Tyrosin und Tryptophan konkurrieren dort am LAT1-Transporter mit verzweigtkettigen Aminosäuren (Leucin, Isoleucin, Valin). Wenn diese erhöht sind, gelangen weniger Dopamin- und Serotonin-Vorstufen ins Gehirn, selbst bei normalen Blutspiegeln.
Ein zusätzlicher Faktor: Die Umwandlung von Phenylalanin zu Tyrosin erfordert Tetrahydrobiopterin (BH4) als Cofaktor. BH4 wird bei oxidativem Stress verbraucht, der bei ADHS (wie im nächsten Abschnitt beschrieben) chronisch erhöht ist. Das bedeutet: Selbst wenn genug Phenylalanin vorhanden ist, kann die Umwandlung zu Tyrosin stocken.
Tryptophan und der Kynurenin-Pathway: Wenn Serotonin-Vorstufen falsch abgebaut werden
Tryptophan ist die Vorstufe von Serotonin. Aber nur etwa 5 Prozent des Tryptophans werden tatsächlich zu Serotonin umgewandelt. Der Grossteil (ca. 95 Prozent) wird über den sogenannten Kynurenin-Pathway metabolisiert, und genau hier liegt bei ADHS ein zentrales Problem.
Eine Metaanalyse von Cavaleri et al. (2024), die 8 Studien mit insgesamt 1.177 Teilnehmenden (707 ADHS, 470 Kontrollen) auswertete, fand: ADHS-Betroffene haben signifikant höheres Kynurenin (SMD = 0,56, p = 0,033) und signifikant niedrigere Kynureninsäure (SMD = -0,33, p < 0,001).
Warum ist das wichtig? Kynureninsäure ist neuroprotektiv: Sie blockiert den NMDA-Rezeptor und schützt so vor Glutamat-Exzitotoxizität (ähnlich wie Magnesium). Weniger Kynureninsäure bedeutet weniger Neuroprotektion. Gleichzeitig kann erhöhtes Kynurenin über neurotoxische Metabolite wie Quinolinsäure (ein NMDA-Rezeptor-Agonist) Nervenzellen schädigen.
Aarsland et al. (2015) bestätigten das Muster bei 133 ADHS-Erwachsenen vs. 131 Kontrollen: signifikant niedrigeres Tryptophan (77,3 vs. 83,6 µmol/L, p = 0,004), niedrigere Kynureninsäure (p = 0,03) und niedrigere Xanthurensäure (p = 0,004). Die Autoren fanden ausserdem niedrigere B2- und B6-Spiegel und interpretierten das als Nährstoffmangel-bedingte Verschiebung des Kynurenin-Metabolismus.
Die Verbindung zum Darm ist hier besonders relevant: Bestimmte Darmbakterien (Alistipes, Bacteroides), die bei ADHS häufig erhöht sind, können Tryptophan direkt im Darm verbrauchen, bevor es überhaupt ins Blut gelangt. Das bedeutet: Weniger Tryptophan für Serotonin, weniger für neuroprotektive Kynureninsäure, mehr für neurotoxische Metabolite.
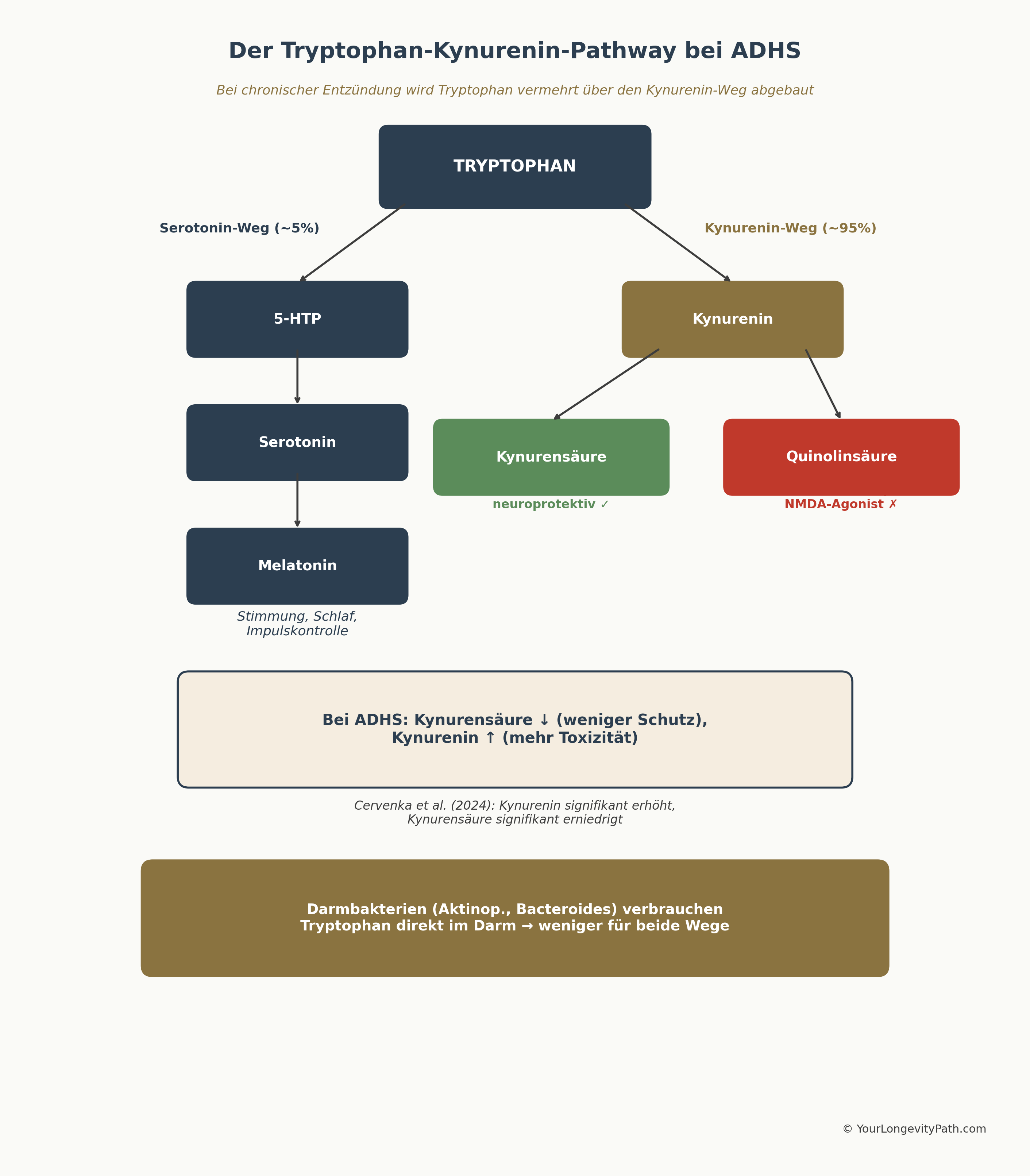 Abbildung 2: Der Tryptophan-Kynurenin-Pathway. Bei chronischer Entzündung wird Tryptophan vermehrt über den Kynurenin-Weg abgebaut — weniger Serotonin, weniger Neuroprotektion. Eigene Darstellung basierend auf Cavaleri et al. (2024), © YourLongevityPath.com
Abbildung 2: Der Tryptophan-Kynurenin-Pathway. Bei chronischer Entzündung wird Tryptophan vermehrt über den Kynurenin-Weg abgebaut — weniger Serotonin, weniger Neuroprotektion. Eigene Darstellung basierend auf Cavaleri et al. (2024), © YourLongevityPath.com
Die Grafik verdeutlicht, warum Entzündungsprozesse bei ADHS so problematisch sind: Sie verschieben die Tryptophan-Verwertung weg vom Serotonin-Weg hin zum Kynurenin-Weg — mit weniger Schutz und mehr Toxizität als Resultat.
Empfohlene Tests: Tryptophan (Serum), Kynurenin, Kynureninsäure. Diese Werte werden im Rahmen einer erweiterten Aminosäure-Analyse gemessen und sind nicht Bestandteil des Standard-Blutbilds.
Glutamin und Glutamat: Das Erregungs-Gleichgewicht
Glutamat ist der stärkste erregende Neurotransmitter im Gehirn. Glutamin ist sein “Recycling-Partner”: In Astrozyten wird überschüssiges Glutamat zu Glutamin umgewandelt, um die Erregung zu dämpfen. Bei ADHS ist dieses Gleichgewicht gestört.
Skalny et al. (2021) untersuchten 71 ADHS-Kinder und 31 Kontrollen und fanden: Glutamat war um 7 Prozent erhöht (p = 0,039), Glutamin um 10 Prozent erniedrigt (p = 0,024), und die Glutamin/Glutamat-Ratio war um 28 Prozent verschoben (p < 0,001). In der Regressionsanalyse korrelierten Glutamatspiegel positiv und Glutaminspiegel negativ mit der ADHS-Symptomschwere.
Das passt direkt zum Magnesiummangel-Thema: Magnesium blockiert den NMDA-Rezeptor, der auf Glutamat reagiert. Wenn Magnesium fehlt und gleichzeitig Glutamat erhöht ist, entsteht eine doppelte Exzitotoxizität, die Nervenzellen schädigt.
Miniksar et al. (2022) bestätigten in einer unabhängigen Studie (46 ADHS-Kinder, 30 Kontrollen), dass erhöhte Serum-Glutamat-Werte als Biomarker für ADHS dienen können, unabhängig von Schlafproblemen.
Empfohlene Tests: Glutamin und Glutamat (Plasma-Aminosäureprofil), Glutamin/Glutamat-Ratio.
GABA: Der inhibitorische Gegenspieler
GABA (Gamma-Aminobuttersäure) wird aus Glutamat synthetisiert und ist der wichtigste hemmende Neurotransmitter. Er bremst neuronale Überaktivität, genau das, was bei ADHS fehlt.
Mehrere Magnetresonanzspektroskopie-Studien (MRS) zeigen reduzierte GABA-Konzentrationen im Gehirn bei ADHS: Edden et al. (2012), veröffentlicht in JAMA Psychiatry, fanden signifikant niedrigere GABA-Spiegel bei ADHS-Kindern. Bollmann et al. (2020) bestätigten reduziertes striatales GABA bei unmedizierten ADHS-Kindern mittels hochauflösendem 7-Tesla-MRT.
Das Paradox: Im Serum fanden Miniksar et al. (2022) erhöhte GABA-Werte. Das deutet darauf hin, dass GABA zwar produziert wird, aber möglicherweise nicht effizient ins Gehirn gelangt oder dort nicht korrekt aufgenommen wird.
Die Verbindung: Wenn Glutamat erhöht und GABA erniedrigt ist, verschiebt sich das Erregungs-/Hemmungs-Gleichgewicht im Gehirn massiv zugunsten der Erregung. Das erklärt Symptome wie Reizüberflutung, Impulsivität und die Schwierigkeit, gedanklich “abzuschalten”.
Histidin: Die unterschätzte Wachheits-Aminosäure
Histidin ist die Vorstufe von Histamin, einem Neurotransmitter, der Wachheit, Aufmerksamkeit und Motivation reguliert. Bornstein et al. (1990) fanden signifikant niedrigere Plasma-Histidinspiegel bei ADD-Patienten. Skalny et al. (2021) beobachteten eine Tendenz zu 29 Prozent niedrigeren Serum-Histidinwerten bei ADHS-Kindern (p = 0,081, knapp nicht signifikant bei kleiner Stichprobe).
Die Evidenz ist hier noch dünn, aber der Mechanismus ist biochemisch plausibel: Ein Histidinmangel könnte die Histamin-Produktion im Gehirn beeinträchtigen und damit zur Aufmerksamkeitsstörung beitragen.
Empfohlene Tests für das Aminosäure-Profil: Ein umfassendes Plasma-Aminosäureprofil (beim Spezialisten) kann Tyrosin, Phenylalanin, Tryptophan, Glutamin, Glutamat, Histidin und die verzweigtkettigen Aminosäuren in einem Durchgang erfassen.
Oxidativer Stress: Wenn die Schutzsysteme überlastet sind
Oxidativer Stress ist kein einzelner Blutwert, sondern ein Zustand, in dem die Produktion reaktiver Sauerstoffspezies (ROS) die antioxidative Kapazität des Körpers übersteigt. Bei ADHS ist dieses Gleichgewicht häufig gestört.
Ceylan et al. (2012) zeigten in einer kontrollierten Studie: Kinder mit ADHS hatten signifikant niedrigere Glutathionperoxidase-Aktivität (GPx) und einen reduzierten totalen Antioxidantienstatus (TAS). Gleichzeitig waren die Malondialdehyd-Spiegel (MDA), ein Marker für Lipidperoxidation (also oxidative Schäden an Zellmembranen), signifikant erhöht. Bulut et al. (2013) fanden bei erwachsenen ADHS-Patienten signifikant erhöhte Malondialdehyd-Werte (ein Marker für Lipidperoxidation) sowie eine signifikant erniedrigte Paraoxonase- und Arylesterase-Aktivität, beides antioxidative Schutzenzyme.
Joseph et al. (2015) fassten den Stand der Forschung zusammen: ADHS-Betroffene zeigen konsistent reduzierte Spiegel von antioxidativen Enzymen (GPx, Katalase, SOD) und einen verminderten totalen Antioxidantienstatus (TOS).
Warum ist der oxidative Stress bei ADHS erhöht?
Mehrere Faktoren laufen zusammen. Die bei ADHS typische chronische sympathische Aktivierung erhöht die ROS-Produktion. Mikronährstoffdefizite (Zink, Magnesium, Selen) schwächen gleichzeitig die antioxidativen Abwehrsysteme, da diese Minerale Cofaktoren der antioxidativen Enzyme sind. Glutathion, das wichtigste intrazelluläre Antioxidans, wird bei chronischem Stress schneller verbraucht als nachproduziert. Und Schlafprobleme, die bei über 70 Prozent der ADHS-Betroffenen auftreten, beeinträchtigen die nächtlichen Reparaturprozesse zusätzlich.
Empfohlene Tests: Glutathion (GSH/GSSG-Ratio), MDA (Malondialdehyd), totaler Antioxidantienstatus (TAS), SOD-Aktivität.
Das Darmmikrobiom: Die Darm-Hirn-Achse bei ADHS
Die Forschung zur Darm-Hirn-Achse bei ADHS hat in den letzten Jahren enorm an Dynamik gewonnen. Ein systematischer Review von Sukmajaya et al. (2021) und eine aktuelle Übersichtsarbeit von Mancini et al. (2025) in Neuroscience zeigen ein zunehmend klares Bild: Die Zusammensetzung des Darmmikrobioms unterscheidet sich bei ADHS-Betroffenen messbar von der gesunder Kontrollen.
Was im Stuhltest auffällt:
Reduzierte Diversität. Mehrere Studien zeigen eine geringere mikrobielle Artenvielfalt bei ADHS, ein Muster, das auch bei anderen entzündlichen und neuropsychiatrischen Erkrankungen beobachtet wird.
Verminderte Faecalibacterium-Abundanz. Faecalibacterium prausnitzii ist einer der wichtigsten Butyratproduzenten im Darm. Butyrat ist eine kurzkettige Fettsäure, die die Darmbarriere stärkt, Entzündungen hemmt und die Blut-Hirn-Schranke schützt. Mehrere Studien fanden konsistent reduzierte Faecalibacterium-Spiegel bei ADHS, mit einer negativen Korrelation zwischen Faecalibacterium-Abundanz und der Schwere von ADHS-Symptomen.
Verändertes Bifidobakterien-Profil. Die Datenlage zu Bifidobakterien ist komplex: Einige Studien finden reduzierte, andere erhöhte Bifidobacterium-Spiegel bei ADHS. Eine aktuelle Studie (BMC Microbiology, 2025) fand signifikant niedrigere Abundanz des Phylum Actinobacteria (zu dem Bifidobacterium gehört) bei behandlungsnaiven ADHS-Kindern.
Erhöhte Bacteroides und Desulfovibrio. Bacteroides-Spezies und Desulfovibriota waren in mehreren Studien bei ADHS erhöht. Desulfovibrio produziert Schwefelwasserstoff (H₂S), der die Darmbarriere schädigen und Entzündungsreaktionen fördern kann.
Warum ist das Mikrobiom bei ADHS verändert?
Die Ursachen sind wahrscheinlich bidirektional. Einerseits begünstigen ADHS-typische Ernährungsmuster (hoher Anteil verarbeiteter Lebensmittel, wenig Ballaststoffe, unregelmässige Mahlzeiten) eine Dysbiose. Andererseits kann eine gestörte Darmflora über die Darm-Hirn-Achse ADHS-Symptome verstärken. Mancini et al. (2025) beschreiben einen plausiblen Mechanismus: Dysbiose führt zu erhöhter intestinaler Permeabilität (“Leaky Gut”), wodurch bakterielle Produkte wie Lipopolysaccharide (LPS) in den Blutkreislauf gelangen. Diese LPS aktivieren periphere Immunzellen, die proinflammatorische Zytokine freisetzen. Diese Zytokine können wiederum die Blut-Hirn-Schranke schädigen und neuroinflammatorische Prozesse im Gehirn auslösen, die Dopamin- und Noradrenalinsignale stören.
Eine Studie fand bei ADHS-Kindern erhöhte Plasma-Spiegel von Lipopolysaccharid-bindendem Protein (LBP), ein indirekter Marker für erhöhte Darmpermeabilität.
Empfohlene Tests: Umfassende Stuhlanalyse mit Mikrobiom-Profiling (16S-rRNA-Sequenzierung), Calprotectin (Entzündungsmarker), Zonulin oder Occludin (Marker für intestinale Permeabilität), kurzkettige Fettsäuren (Butyrat, Propionat, Acetat), Alpha-1-Antitrypsin.
Warum das alles zusammenhängt: Der biologische Teufelskreis
Diese einzelnen Defizite existieren nicht isoliert. Sie bilden ein Netzwerk, das sich gegenseitig verstärkt.
Magnesiummangel verstärkt die Stressreaktion (Sartori et al., 2012), was mehr Cortisol bedeutet. Mehr Cortisol erhöht den Verbrauch von Zink und Magnesium. Gleichzeitig stört chronischer Stress das Darmmikrobiom. Ein gestörtes Mikrobiom produziert weniger Butyrat, was die Darmbarriere schwächt. Eine durchlässige Darmbarriere lässt Entzündungsmediatoren durch, die oxidativen Stress erhöhen. Oxidativer Stress verbraucht Glutathion und Antioxidantien. Und ohne ausreichend Antioxidantien werden die Zellmembranen geschädigt, was die Aufnahme von Omega-3-Fettsäuren und anderen Nährstoffen weiter beeinträchtigt.
Ein weiteres Beispiel: Viele Betroffene supplementieren hochdosiertes Vitamin D. Doch um Vitamin D in seine aktive Form umzuwandeln, braucht der Körper zwingend Magnesium. Wer bei einem versteckten Magnesiummangel hohe Dosen Vitamin D einnimmt, entleert seine Magnesiumspeicher noch weiter, und die innere Unruhe nimmt plötzlich zu.
Stimulanzien können diesen Kreislauf zusätzlich befeuern: Sie unterdrücken den Appetit (weniger Nährstoffzufuhr), erhöhen den Magnesiumverbrauch (Schmidt et al., 1994) und können über die sympathische Aktivierung den oxidativen Stress verstärken.
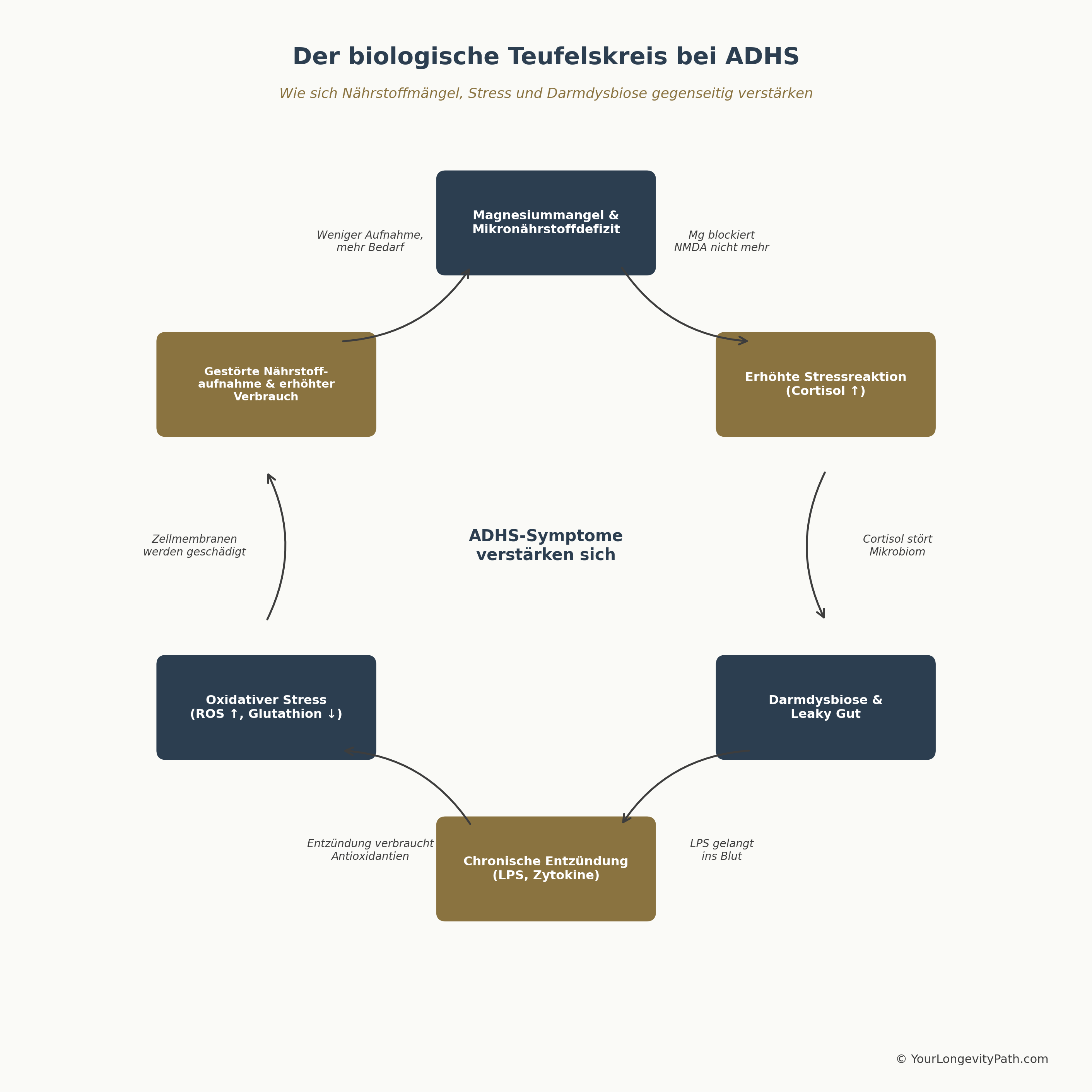 Abbildung 3: Der biologische Teufelskreis bei ADHS. Mikronährstoffmängel, Stress, Darmdysbiose und oxidativer Stress verstärken sich gegenseitig. Eigene Darstellung, © YourLongevityPath.com
Abbildung 3: Der biologische Teufelskreis bei ADHS. Mikronährstoffmängel, Stress, Darmdysbiose und oxidativer Stress verstärken sich gegenseitig. Eigene Darstellung, © YourLongevityPath.com
Die Grafik zeigt, warum isolierte Massnahmen oft nicht reichen: Wer nur Magnesium supplementiert, aber den entzündeten Darm ignoriert, durchbricht den Kreislauf nicht. Ein wirksamer Ansatz muss an mehreren Stellen gleichzeitig ansetzen.
Was du konkret tun kannst
Wenn du ADHS hast und das Gefühl, dass dir “etwas fehlt”, obwohl du vielleicht schon Medikamente nimmst, hier ist ein strukturierter Ansatz. Wichtig dabei: Nicht alles auf einmal. Teile es in machbare Schritte auf.
WICHTIG: Niemals blind supplementieren. Besonders Eisen, Zink und Kupfer dürfen nur nach einem nachgewiesenen Mangel im Bluttest eingenommen werden, da ein Überschuss hier toxisch wirken und den oxidativen Stress massiv erhöhen kann. Eisen ohne bestätigten Mangel zu supplementieren, kann zu Organschäden führen. Auch beim Kupfer-Zink-Verhältnis gilt: Zink isoliert zu geben, ohne den Kupferstatus zu kennen, kann das Gleichgewicht in die falsche Richtung verschieben. Immer erst testen, dann handeln.
Priorisiere deine Labortests (vermeide Überforderung)
Niemand muss alles auf einmal testen. Teile es in zwei machbare Schritte auf:
Schritt 1: Das Basis-Panel (oft beim Hausarzt möglich). Ferritin und Transferrinsättigung (Eisenspeicher), CRP (Entzündungsmarker, um falsch-hohe Ferritinwerte auszuschliessen), 25(OH)D (Vitamin D), Holotranscobalamin (aktives Vitamin B12, sensitiver als Gesamt-B12), Folat (Erythrozytenfolat ist aussagekräftiger als Serumfolat), Homocystein (Marker für die Effizienz des Methylierungszyklus) und der Omega-3-Index.
Schritt 2: Das funktionelle Panel (beim Spezialisten). Vollblut-Magnesium (nicht Serum, da der Serumwert einen intrazellulären Mangel nicht ausschliesst), Serum-Zink, Serum-Kupfer und die Kupfer/Zink-Ratio, Vitamin B6, Plasma-Aminosäureprofil (Tyrosin, Phenylalanin, Tryptophan, Glutamin, Glutamat, Histidin) sowie eine umfassende Mikrobiom-Stuhlanalyse. Bei der Stuhlanalyse sind besonders relevant: Mikrobiom-Diversität, Faecalibacterium prausnitzii, kurzkettige Fettsäuren (Butyrat, Propionat, Acetat) und Entzündungsmarker wie Calprotectin und Zonulin.
 Abbildung 4: Welche Tests in welcher Reihenfolge sinnvoll sind. Schritt 1 ist oft beim Hausarzt möglich, Schritt 2 erfordert einen funktionell orientierten Spezialisten. Eigene Darstellung, © YourLongevityPath.com
Abbildung 4: Welche Tests in welcher Reihenfolge sinnvoll sind. Schritt 1 ist oft beim Hausarzt möglich, Schritt 2 erfordert einen funktionell orientierten Spezialisten. Eigene Darstellung, © YourLongevityPath.com
Besprich die Ergebnisse mit jemandem, der sie einordnen kann. Laborwerte im Referenzbereich sind nicht automatisch optimal. Der Referenzbereich beschreibt, wo 95 Prozent der Bevölkerung liegen, nicht wo die Werte liegen sollten, damit dein Gehirn optimal funktioniert. Ein funktionell orientierter Arzt oder Coach kann die Werte im Kontext deiner Symptome und deiner Medikation interpretieren.
Beginne nicht mit zehn Supplementen gleichzeitig. Wie ich in meinem Beitrag Schritt für Schritt statt alles auf einmal erklärt habe: Eine Veränderung zur Zeit ist der Weg, der funktioniert. Identifiziere dein grösstes Defizit und adressiere es gezielt.
Fazit
ADHS ist nicht nur eine Frage der Neurotransmitter. Es ist eine systemische Angelegenheit, bei der Mikronährstoffdefizite, Aminosäure-Dysbalancen, oxidativer Stress und Darm-Hirn-Achsen-Dysfunktion ineinandergreifen. Die Forschung zeigt messbare Abweichungen in Magnesium, Eisen (Ferritin), Zink, Kupfer, Vitamin D, Omega-3-Fettsäuren, B-Vitaminen, Aminosäuren (Tryptophan-Kynurenin-Pathway, Glutamin/Glutamat-Ratio, GABA), antioxidativer Kapazität und der Zusammensetzung des Darmmikrobioms.
Das bedeutet nicht, dass jeder Mensch mit ADHS alle diese Defizite hat. Aber es bedeutet, dass ein gezieltes Screening sinnvoll ist. Denn wenn du ein neurologisches System optimieren willst, das unter Dauerstress steht, musst du ihm die Rohstoffe geben, die es braucht. Medikamente können den Dopaminspiegel im synaptischen Spalt anheben. Aber sie können kein Eisen liefern, aus dem Dopamin hergestellt wird. Sie können die NMDA-Rezeptoren nicht stabilisieren, wenn Magnesium fehlt. Und sie können keine entzündete Darmbarriere reparieren.
Die gute Nachricht: Diese Parameter sind messbar, und viele von ihnen sind beeinflussbar. Nicht mit einer Wunderpille, sondern mit einem strukturierten, evidenzbasierten Ansatz, der dort ansetzt, wo dein Körper den grössten Bedarf hat.
Wer tiefer in das Thema Magnesium und ADHS einsteigen möchte: In meinem Beitrag ADHS und Magnesium L-Threonat erkläre ich ausführlich, warum eine bestimmte Magnesiumform für das ADHS-Gehirn besonders relevant ist.
Wissenschaftliche Quellen
Aarsland, T. I., Landaas, E. T., Hegvik, T. A., et al. (2015). Serum concentrations of kynurenines in adult patients with attention-deficit hyperactivity disorder (ADHD): a case–control study. Behavioral and Brain Functions, 11, 36. doi: 10.1186/s12993-015-0080-x
Altun, H., Kurutas, E. B., Sahin, N., Gungor, O., & Findikli, E. (2018). The levels of vitamin B6, folate, and vitamin B12 in boys with attention deficit hyperactivity disorder. Zeitschrift für Kinder- und Jugendpsychiatrie und Psychotherapie, 46(5), 396–404. doi: 10.1024/1422-4917/a000559
Arnold, L. E., Bozzolo, H., Hollway, J., et al. (2005). Serum zinc correlates with parent- and teacher-rated inattention in children with attention-deficit/hyperactivity disorder. Journal of Child and Adolescent Psychopharmacology, 15(4), 628–636. doi: 10.1089/cap.2005.15.628
Bergwerff, C. E., Luman, M., Blom, H. J., & Oosterlaan, J. (2016). No Tryptophan, Tyrosine and Phenylalanine Abnormalities in Children with Attention-Deficit/Hyperactivity Disorder. PLOS ONE, 11(3), e0151100. doi: 10.1371/journal.pone.0151100
Bollmann, S., Ghisleni, C., Poil, S. S., et al. (2020). Reduced striatal GABA in unmedicated children with ADHD at 7T. Psychiatry Research: Neuroimaging, 301, 111082. doi: 10.1016/j.pscychresns.2020.111082
Bornstein, R. A., Baker, G. B., Carroll, A., et al. (1990). Plasma amino acids in attention deficit disorder. Psychiatry Research, 33(3), 301–306. doi: 10.1016/0165-1781(90)90046-8
Bulut, M., Selek, S., Bez, Y., et al. (2013). Lipid peroxidation markers in adult attention deficit hyperactivity disorder: New findings for oxidative stress. Psychiatry Research, 209(3), 638–642. doi: 10.1016/j.psychres.2013.02.025
Cavaleri, D., Crocamo, C., Morello, P., Bartoli, F., & Carrà, G. (2024). The kynurenine pathway in attention-deficit/hyperactivity disorder: A systematic review and meta-analysis of blood concentrations of tryptophan and its catabolites. Journal of Clinical Medicine, 13(2), 583. doi: 10.3390/jcm13020583
Ceylan, M. F., Sener, S., Bayraktar, A. C., & Kavutcu, M. (2012). Changes in oxidative stress and cellular immunity serum markers in attention-deficit/hyperactivity disorder. Psychiatry and Clinical Neurosciences, 66(3), 220–226. doi: 10.1111/j.1440-1819.2012.02330.x
Chang, J. P. C., Su, K. P., Mondelli, V., & Pariante, C. M. (2018). Omega-3 polyunsaturated fatty acids in youths with attention deficit hyperactivity disorder: A systematic review and meta-analysis. Neuropsychopharmacology, 43(3), 534–545. doi: 10.1038/npp.2017.160
Cortese, S., Angriman, M., Lecendreux, M., & Konofal, E. (2012). Iron and attention deficit/hyperactivity disorder: What is the empirical evidence so far? Expert Review of Neurotherapeutics, 12(10), 1227–1240. doi: 10.1586/ern.12.116
Edden, R. A. E., Crocetti, D., Zhu, H., Gilbert, D. L., & Mostofsky, S. H. (2012). Reduced GABA concentration in attention-deficit/hyperactivity disorder. Archives of General Psychiatry (now JAMA Psychiatry), 69(7), 750–753. doi: 10.1001/archgenpsychiatry.2011.2280
Effatpanah, M., Rezaei, M., Effatpanah, H., et al. (2019). Magnesium status and attention deficit hyperactivity disorder (ADHD): A meta-analysis. Psychiatry Research, 274, 228–234. doi: 10.1016/j.psychres.2019.02.040
Ghoreishy, S. M., Ebrahimi Mousavi, S., Asoudeh, F., & Mohammadi, H. (2021). Zinc status in attention-deficit/hyperactivity disorder: A systematic review and meta-analysis of observational studies. Scientific Reports, 11, 14612. doi: 10.1038/s41598-021-94124-5
Yektaş, Ç., Alpay, M., & Tufan, A. E. (2019). Comparison of serum B12, folate and homocysteine concentrations in children with autism spectrum disorder or attention deficit hyperactivity disorder and healthy controls. Neuropsychiatric Disease and Treatment, 15, 2213–2219. doi: 10.2147/NDT.S212361
Huang, Y. H., Zeng, B. Y., Li, D. J., et al. (2019). Significantly lower serum and hair magnesium levels in children with attention deficit hyperactivity disorder than controls: A systematic review and meta-analysis. Progress in Neuro-Psychopharmacology and Biological Psychiatry, 90, 134–141. doi: 10.1016/j.pnpbp.2018.11.012
Schmidt, M. E., Kruesi, M. J. P., Elia, J., Borcherding, B. G., Elin, R. J., Hosseini, J. M., McFarlin, K. E., & Hamburger, S. D. (1994). Effect of dextroamphetamine and methylphenidate on calcium and magnesium concentration in hyperactive boys. Psychiatry Research, 54(2), 199–210. doi: 10.1016/0165-1781(94)90006-X
Joseph, N., Zhang-James, Y., Perl, A., & Faraone, S. V. (2015). Oxidative stress and ADHD: A meta-analysis. Journal of Attention Disorders, 19(11), 915–924. doi: 10.1177/1087054713510354
Khoshbakht, Y., Bidaki, R., & Salehi-Abargouei, A. (2018). Vitamin D status and attention deficit hyperactivity disorder: A systematic review and meta-analysis of observational studies. Advances in Nutrition, 9(1), 9–20. doi: 10.1093/advances/nmx002
Kozielec, T., & Starobrat-Hermelin, B. (1997). Assessment of magnesium levels in children with attention deficit hyperactivity disorder (ADHD). Magnesium Research, 10(2), 143–148. PMID: 9368235
LaChance, L., McKenzie, K., Taylor, V. H., & Vigod, S. N. (2016). Omega-6 to omega-3 fatty acid ratio in patients with ADHD: A meta-analysis. Journal of the Canadian Academy of Child and Adolescent Psychiatry, 25(2), 87–96. PMID: 27274744
Mancini, V. O., et al. (2025). Gut dysbiosis as a driver of neuroinflammation in attention-deficit/hyperactivity disorder: A review of current evidence. Neuroscience, 569, 298–312. doi: 10.1016/j.neuroscience.2025.01.024
Miniksar, D. Y., Özdem, S., & Guseinova, N. (2022). GABA, glutamate and homocysteine serum levels and their association with aggression, impulsivity and inattention in children with ADHD. Psychiatry Research, 311, 114473. doi: 10.1016/j.psychres.2022.114473
Pickering, G., Mazur, A., Trousselard, M., et al. (2020). Magnesium status and stress: The vicious circle concept revisited. Nutrients, 12(12), 3672. doi: 10.3390/nu12123672
Sartori, S. B., Whittle, N., Hetzenauer, A., & Singewald, N. (2012). Magnesium deficiency induces anxiety and HPA axis dysregulation: Modulation by therapeutic drug treatment. Neuropharmacology, 62(1), 304–312. doi: 10.1016/j.neuropharm.2011.07.027
Skalny, A. V., Mazaletskaya, A. L., Ajsuvakova, O. P., et al. (2021). Serum amino acid spectrum in children with attention deficit hyperactivity disorder (ADHD). Journal of Trace Elements in Medicine and Biology, 65, 126717. doi: 10.1016/j.jtemb.2021.126717
Sukmajaya, A. C., Lusida, M. I., Soetjipto, S., & Setiawati, Y. (2021). Systematic review of gut microbiota and attention-deficit hyperactivity disorder (ADHD). Annals of General Psychiatry, 20(1), 12. doi: 10.1186/s12991-021-00330-w
Skalny, A. V., Mazaletskaya, A. L., Ajsuvakova, O. P., Bjørklund, G., Skalnaya, M. G., Chao, J. C.-J., Chernova, L. N., Shakieva, R. A., Kopylov, P. Yu., & Tinkov, A. A. (2020). Serum zinc, copper, zinc-to-copper ratio, and other essential elements and minerals in children with attention deficit/hyperactivity disorder (ADHD). Journal of Trace Elements in Medicine and Biology, 58, 126445. doi: 10.1016/j.jtemb.2019.126445
Wang, Y., Huang, L., Zhang, L., et al. (2017). Peripheral iron levels in children with attention-deficit hyperactivity disorder: A systematic review and meta-analysis. Scientific Reports, 7(1), 14029. doi: 10.1038/s41598-017-19096-x
Welche Blutwerte sollte man bei ADHS testen lassen?
Ferritin, Zink, Magnesium (Vollblut), Vitamin D, Omega-3-Index und Homocystein. Standard-Blutbilder erfassen diese Werte meist nicht — sie müssen gezielt angefordert werden.
Kann ein Nährstoffmangel ADHS-Symptome verschlimmern?
Ja. Magnesium, Eisen, Zink und Omega-3 sind direkt an der Dopamin- und Noradrenalin-Synthese beteiligt. Ein Mangel kann Konzentration, Impulskontrolle und Reizfilterung messbar verschlechtern.
Warum spielt der Darm bei ADHS eine Rolle?
Über 90 % des Serotonins werden im Darm produziert. Eine Dysbiose stört die Nährstoffaufnahme und erhöht Entzündungsmarker, die direkt auf die Hirnfunktion wirken.
Dieser Artikel dient ausschliesslich der Information und ersetzt keine ärztliche Beratung, Diagnose oder Behandlung. Bei gesundheitlichen Beschwerden wende dich bitte an eine qualifizierte medizinische Fachperson.